L'homéopathie controversée aux Etats-Unis
Publié le 23 avril 2015 à 15:55
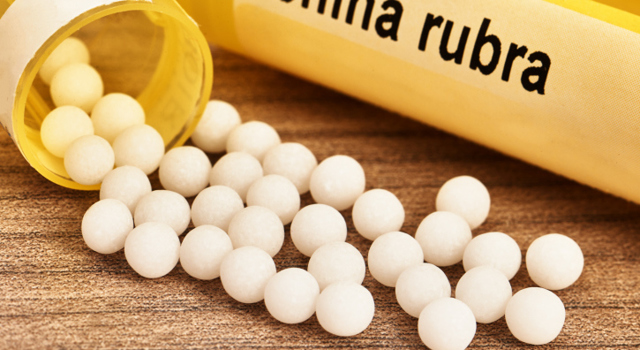
Aux Etats-Unis, la mise sur le marché des médicaments homéopathiques n’est pas contrôlée, ce qui suscite une polémique dans les milieux médicaux quant à son efficacité et à son innocuité. Mais qu’en est-il en France ?
Selon un article de Sciences et Avenir publié le 23 avril, l'efficacité et l'innocuité de l’homéopathie seraient controversées aux États-Unis.
En effet, aux USA, la FDA (Agence du médicament américaine) ne contrôle pas la mise sur le marché des médicaments homéopathiques comme elle le fait pour les médicaments.
De ce fait, certains accidents avaient eu lieu avec des médicaments homéopathiques comme le Zicam®, un traitement contre le rhume, avec plus de 130 personnes qui avaient perdu l'odorat en 2009.
En mars 2015, la FDA avait d’ailleurs mis en garde le public américain contre le risque potentiel de produits homéopathiques pour traiter l'asthme vendus sans ordonnance car leur efficacité et leur innocuité n'avaient pas été évaluées.
Pour faire face à ce problème, l'Agence américaine vient de terminer 2 jours d'auditions publiques pour déterminer la nécessité de renforcer la réglementation de ce marché de plusieurs milliards de dollars : « Les informations obtenues durant ce comité consultatif d'experts indépendants aideront la FDA à déterminer la pertinence et la clarté des textes actuels pour réglementer les produits homéopathiques, dont le marché a connu une croissance explosive ces vingt-cinq dernières années », a conclu la FAD.
En France, comment cela se passe-t-il ?
Dans notre pays, les médicaments homéopathiques sont obligés de passer par une demande de mise sur le marché (AMM) auprès de l’Agence nationale de sécurité du médicament et des produits de santé (ANSM).
Cette demande est accompagnée d’un dossier documentant la qualité, la sécurité et l’usage homéopathique du médicament. Après évaluation de ce dossier et si le médicament présente les garanties requises, l’ANSM peut, selon le cas, délivrer l’AMM ou procéder à l’enregistrement du médicament homéopathique.
Une fois commercialisés, les médicaments homéopathiques, quel que soit leur régime réglementaire de mise sur le marché, sont soumis à la pharmacovigilance afin, notamment de surveiller le risque d’effets indésirables éventuels résultant de leur utilisation.
Infos pratiques
Pour en savoir plus : médicamentshoméopathiques.gouv.fr (site du ministère de la santé)
Auteur: Nathalie
- Publicité -
- Publicité -
 Santé en 2026 : les tendances à suivre
Santé en 2026 : les tendances à suivre
 Actualité santé : les infos essentielles pour prendre soin de soi
Actualité santé : les infos essentielles pour prendre soin de soi
 Analyses médicales : comment bien interpréter ses résultats ?
Analyses médicales : comment bien interpréter ses résultats ?






